La Tabla Periódica es una de las herramientas más fundamentales en la química, actuando como un catálogo que organiza los elementos químicos conocidos de manera sistemática. Comprender su estructura y significado no solo es crucial para los estudiantes de química, sino también para cualquier persona interesada en las ciencias naturales. En este artículo, exploraremos la historia, la organización y la importancia de la Tabla Periódica, así como aspectos curiosos que la rodean.
¿Qué es la tabla periódica y su significado?
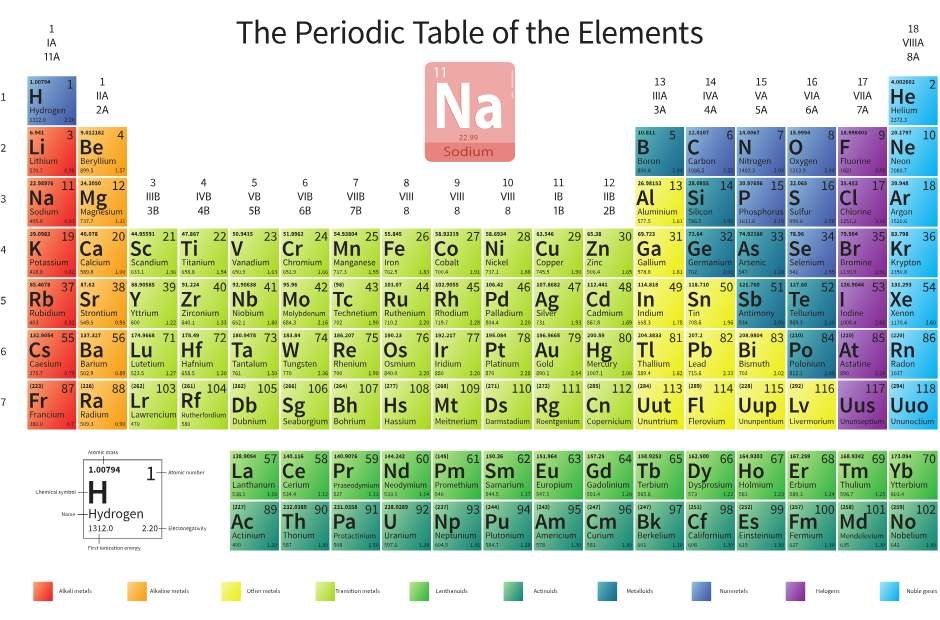
La Tabla Periódica de los elementos es un compendio que reúne todos los elementos químicos que ha descubierto la humanidad. Estos elementos están dispuestos en un formato tabular, donde cada uno se identifica por su número atómico, que se define como la cantidad de protones presentes en el núcleo del átomo. Este ordenamiento permite establecer patrones en las propiedades químicas y físicas de los elementos.
La materia que compone nuestro universo —desde el aire que respiramos hasta los metales que utilizamos— está formada por combinaciones de estos 118 elementos. Cada elemento tiene un símbolo químico único, que a menudo es una abreviatura del nombre del elemento en latín o griego. Por ejemplo, el oxígeno se representa como O, y el oro como Au.
Además, cada elemento se clasifica según su estado de agregación a temperaturas y presiones normales: sólido, líquido o gas. Esta clasificación es esencial para entender cómo los elementos interactúan entre sí y cómo forman compuestos.
Historia de la tabla periódica
La Tabla Periódica actual tiene sus raíces en el trabajo de varios científicos a lo largo de la historia. El primer intento de organizar los elementos químicos fue realizado por el químico ruso Dmitri Mendeléyev en 1869. Su versión contenía 63 elementos, organizados de acuerdo a sus propiedades químicas. Mendeléyev fue pionero al dejar espacios vacíos en su tabla anticipando la existencia de elementos aún por descubrir.
En 1871, Mendeléyev presentó una versión revisada que agrupaba los elementos en columnas basándose en sus propiedades comunes, un enfoque que todavía se refleja en la tabla moderna. Mientras tanto, el químico alemán Julius Lothar Meyer también desarrolló una tabla, pero centrada en las propiedades físicas de los elementos.
Con el tiempo, la tabla pasó por varias actualizaciones, siendo una de las más significativas la versión publicada en 1923 por el químico estadounidense Horace Groves Deming, que introdujo 18 columnas identificadas, formando la base de la estructura que utilizamos hoy en día.
Organización de la tabla periódica
La tabla periódica está organizada en siete filas, conocidas como períodos, y 18 columnas, llamadas grupos o familias. En esta disposición, los elementos se ordenan en función de su número atómico, lo que significa que el número atómico aumenta de izquierda a derecha en cada período y de arriba hacia abajo en cada grupo.
Los grupos son clave para entender las propiedades químicas de los elementos. A continuación, se presentan los principales grupos de la tabla periódica:
- Grupo 1 (IA): Metales alcalinos: litio (Li), sodio (Na), potasio (K), entre otros.
- Grupo 2 (IIA): Metales alcalinotérreos: berilio (Be), magnesio (Mg), calcio (Ca).
- Grupo 13 (IIIA): Térreos: boro (B), aluminio (Al), galio (Ga).
- Grupo 14 (IVA): Carbonoides: carbono (C), silicio (Si), plomo (Pb).
- Grupo 15 (VA): Nitrogenoides: nitrógeno (N), fósforo (P), arsénico (As).
- Grupo 16 (VIA): Calcógenos: oxígeno (O), azufre (S), selenio (Se).
- Grupo 17 (VIIA): Halógenos: flúor (F), cloro (Cl), bromo (Br).
- Grupo 18 (VIIIA): Gases nobles: helio (He), neón (Ne), argón (Ar).
Elementos de la tabla periódica: un vistazo más profundo
Los 118 elementos de la tabla periódica se dividen en diferentes categorías según sus propiedades y características. Aparte de los grupos mencionados, hay que considerar:
- Metales: La mayoría de los elementos son metales, conocidos por su conductividad eléctrica y térmica.
- No metales: Gases como el oxígeno y el nitrógeno, que no conducen electricidad y tienen propiedades muy diversas.
- Metaloides: Elementos que tienen propiedades intermedias entre metales y no metales, como el silicio y el germanio.
Es importante mencionar que, además de sus propiedades, los elementos pueden clasificarse según su abundancia en la naturaleza, su reactividad y su estado físico en condiciones normales.
¿Cuántos elementos tiene la tabla periódica y cuáles son?
Actualmente, la tabla periódica contiene 118 elementos, desde el hidrógeno (H), que es el más ligero, hasta el oganesón (Og), uno de los elementos más pesados. A continuación, se presenta una breve lista de algunos de estos elementos destacados:
- Hidrógeno (H)
- Helio (He)
- Litio (Li)
- Carbono (C)
- Nitrógeno (N)
- Oxígeno (O)
- Hierro (Fe)
- Oro (Au)
- Plomo (Pb)
- Uranio (U)
La tabla periódica en diferentes formatos
Con el avance de la tecnología, la tabla periódica ha evolucionado en su presentación y accesibilidad. Hoy en día, se pueden encontrar diferentes versiones y formatos:
- Tabla periódica en PDF: Documentos fáciles de descargar y compartir.
- Tabla periódica para imprimir: Versiones en alta resolución que son ideales para aulas y laboratorios.
- Tabla periódica interactiva: Herramientas en línea que permiten explorar la tabla con información adicional sobre cada elemento.
- Tabla periódica en varios idiomas: Incluyendo versiones en español e inglés para facilitar su uso en todo el mundo.
Importancia de la tabla periódica en la ciencia
La Tabla Periódica es más que una simple lista de elementos. Su estructura permite a los científicos predecir cómo se comportarán los elementos en reacciones químicas, lo que es esencial para el desarrollo de nuevos materiales, medicamentos y tecnologías. Algunos puntos de relevancia incluyen:
- Facilita la enseñanza: Su organización clara ayuda a estudiantes y educadores a comprender las relaciones entre los elementos.
- Investigación científica: Proporciona un marco para el descubrimiento de nuevos elementos y compuestos.
- Aplicaciones prácticas: Ayuda en áreas como la farmacología, la ingeniería de materiales y la biotecnología, donde el conocimiento sobre los elementos es crucial.
Curiosidades sobre la tabla periódica
Existen varios datos curiosos sobre la Tabla Periódica que pueden sorprender incluso a los más conocedores:
- El elemento más abundante: El hidrógeno es el elemento más abundante en el universo, constituyendo aproximadamente el 75% de su materia visible.
- Elementos sintéticos: Algunos elementos en la tabla, como el plutonio (Pu) y el californio (Cf), no se encuentran en la naturaleza y son creados artificialmente en laboratorios.
- El elemento más pesado: El oganesón (Og) es el elemento más pesado conocido, y su existencia es extremadamente inestable.
- Uso cultural: La tabla periódica ha sido objeto de arte, música y literatura, reflejando su influencia más allá de la ciencia.
La Tabla Periódica sigue siendo un símbolo de la ciencia moderna, representando tanto el conocimiento adquirido como las oportunidades futuras en el campo de la química y más allá.